Introducción a las reacciones químicas
Los átomos no suelen encontrarse aislados en la naturaleza. La mayoría necesita completar su último nivel de energía y, para lograrlo, pueden ganar, perder o compartir electrones. Al hacerlo, se unen entre sí y forman moléculas.
Cuando una sustancia está formada únicamente por un mismo tipo de molécula, decimos que es una sustancia pura. Por ejemplo, el agua está compuesta solo por moléculas de H2O.
Si mezclamos dos o más sustancias, los átomos de esas moléculas pueden romper algunas uniones y formar otras nuevas, generando nuevas sustancias. A este proceso se lo llama reacción química.
- Reactivos: las sustancias iniciales que participan en la reacción.
- Productos: las sustancias que se obtienen como resultado de la reacción.
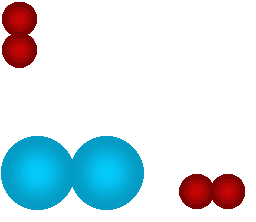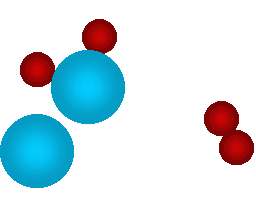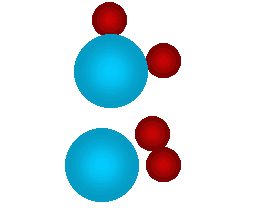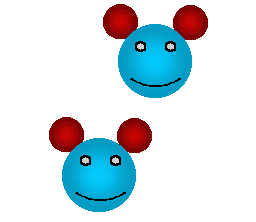
En la siguiente animación observaremos, en forma simplificada, la reacción del hidrógeno (H2) y el oxígeno (O2) para formar agua. A nivel microscópico, se verá cómo las moléculas chocan entre sí: a veces las uniones se rompen y luego los átomos se reacomodan formando nuevas moléculas. Los círculos rojos representan átomos de hidrógenos y los círculos celestes representan átomos de oxígeno.