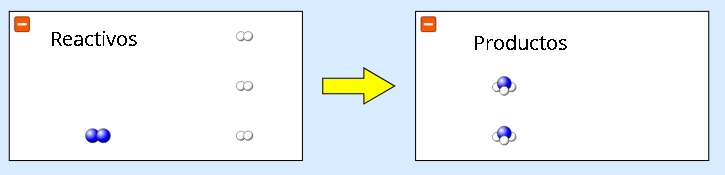
Como hemos visto en la materia, los átomos se juntan para compartir o robar o ceder electrones y llegar a una configuración de electrones de valencia que sea más favorable. En general la estructura atómica más estable es tener 8 electrones de valencia (o 2 para el hidrógeno y el helio). Al juntarse los átomos forman moléculas (con uniones covalentes y/o iónicas) o redes cristalinas (con uniones metálicas).
Una sustancia es una gran cantidad de moléculas iguales. El agua son moléculas de , El azucar de mesa son moléculas de , etc. Cuando se mezclan sustancia puede suceder que se den reacciones químicas que producen nuevas sustancias porque los átomos se ordenan distinto formando otras moléculas.
Una reacción química muy conocida es mezcla del bicarbonato de sodio con vinagre que produce unas burbujas según la reacción
En las reacciones químicas se produce reordenamiento de los átomos de las moléculas en los reactivos para generar otras moléculas. En esta reordenación la cantidad de átomos de cada elemento no cambia. Si inicialmente había 200 átomos de Nitrógeno, luego de la reacción tendrá que seguir existiendo 200 átomos de Nitrógeno.
Para producir agua a partir de Hidrógeno gaseoso y Oxígeno gaseoso debe combinarse de la siguiente manera:
Dos moléculas de gas Hidrógeno (que son 4 átomos de ) y una molécula de gas Oxígeno (que son 2 átomos de ) permiten formar dos moléculas de agua (que tiene en total 4 átomos de y 2 átomos de ). Notar que de cada lado hay la misma cantidad de átomos de cada elemento químico ( y ). A esto se le llama reacción química balanceada.
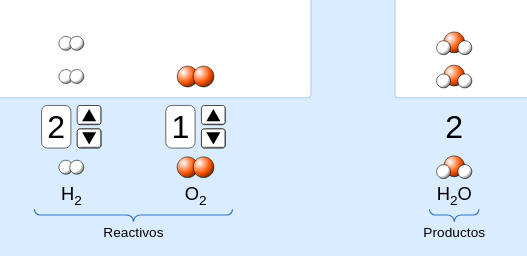
Entrar en la simulación Reactivos, productos y excedentes y explorar sus posibilidades.
Entrar en la pestaña ecuaciones. Buscar el balance de ecuación para cada una de las reacciones de Síntesis, Descomposición (son 8 ecuaciones en total). Si te animás podes hacer las 4 reacciones de combustión. Balancear la ecuación significa buscar la cantidad de moléculas que necesitas de cada reactivo y cada producto para tener la misma cantidad de átomos de cada elemento a cada lado de la ecuación. Una vez encontrado la ecuación balanceada, escribirla en la carpeta y representar todas las moléculas de reactivos y de productos, considerando la cantidad de cada una. Al dibujar los átomos diferenciar con color dependendiendo a que elemento corresponde (Por ejemplo: Hidrógeno con azul, Oxígeno con rojo, Carbono con negro, etc.)
En la carpeta debe terminar la actividad con 8 reacciones balanceadas y su representación esquemáticas de las moléculas.
Por ejemplo, para la reacción balanceada química entre los reactivos y para dar como producto